목차
피비파마 주가 전망에 대해 알아보고 상장 당시 공모가와 '허셉틴 바이오시밀러' 어떻게 진행되고 있는지 확인해 보겠습니다. 피비파마의 정식 기업 명칭은 '프레스티지바이오파마'입니다.
피비파마라고 종목명을 정한 이유는 공식 사명의 글자수가 많아 6자 내외로 권고하는 거래소 지침에 따라 간략하게 표현한 결과라고 합니다.
피비파마(프레스티지바이오파마)는 싱가포르에 위치한 회사로 8종의 바이오시밀러와 2종의 항체신약을 개발하고 있습니다. 지난 달 진행한 공모 청약에서 경쟁률 237대 1로 증거금 11조6400억원을 기록했습니다. 피비파마 주가는 확정 공모가는 희망 공모가 상단인 3만2000원으로 결정됐으며 공모가 기준 공모 자금은 약 4909억원 정도 입니다.

피비파마는 공모 자금을 연구개발 및 시설투자와 더불어 글로벌 시장 진출에 적극 투자할 계획으로, 향후 허셉틴 바이오시밀러(HD201)의 품목 허가 및 췌장암 항체신약(HD1510)의 임상 진행에 주력할 예정이라고 합니다.
피비파마와 같은 추천주 또는 급등주는 여기서 알아보시면 도움이 되실겁니다.
3차 재난 지원금 신청 대상 조회 방법
3차 재난 지원금 신청 대상 조회 방법 2021년 3차 재난 지원금 신청 대상 조회 방법 알아보겠습니다. 전국민 대상으로 재난 지원금을 지급한다면 2020년 재난 지원금 당시 방법으로 진행 될 확률이
dadaminf.tistory.com
현대바이오 주가 전망 '아깝다, 아까워...'
현대바이오 주가 전망에 대해 알아보겠습니다. 현대바이오가 '니클로사마이드' 기반 코로나19 치료제의 효력 실험이 전북대와 공동으로 본격화 된다는 소식에 상한가 마감을 했습니다. 코로나 1
dadaminf.tistory.com
일양약품 주가 전망, '슈펙트' 백혈병 치료제 등록 목표가는?
일양약품 주가 전망, '슈펙트' 백혈병 치료제 등록 목표가는?
일양약품 주가 전망 및 '슈펙트' 백혈병 치료제 급등 이유를 알아보겠습니다. 일양약품의 골수성 백혈병 치료제 '슈펙트'가 러시아 식약청에 백혈병 1차 치료제 등록 절차를 진행 중이라는 소식
dadaminf.tistory.com
피비파마 주가 전망 정리
피비파마 종목 소개
- 피비파마는 2015년 싱가포르에 설립된 이래, 항체의약품 개발 전문 제약회사로 다양한 플랫폼 기술을 기반으로 바이오시밀러 경쟁력의 핵심인 원가경쟁력 향상에 주력하고 있습니다.
- 피비파마는 바이오시밀러와 항체신약을 연구 및 개발하고 있으며 아바스틴 바이오시밀러의 경우 글로벌 임상 3상이 진행 중에 있으며, 휴미라 바이오시밀러는 호주 임상 1상을 위한 IND 승인 신청을 앞두고 있습니다.
피비파마 허셉틴 바이오시밀러
- 피비파마는 파이프라인 중 개발이 가장 앞선 허셉틴 바이오시밀러(HD201)의 경우 품목허가에 필요한 임상 3상 시험을 성공적으로 완료하여, 바이오시밀러 시장이 활성화된 유럽 지역에 판매 승인과 출시를 앞두고 있습니다.
- 현재 피비파마의 허셉틴 바이오시밀러는 글로벌 제약사와의 성공적인 라이선스아웃(License-out) 계약 체결을 통하여 그 시장성 및 기술력을 인정받고 있습니다.
피비파마 연결 회사
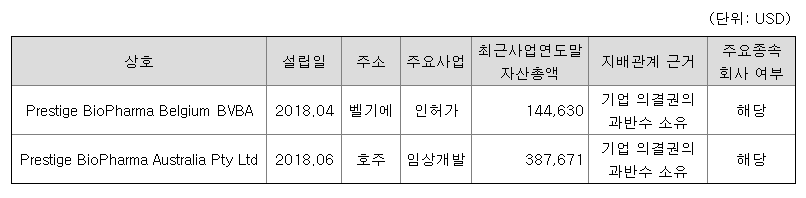
현재 피비파마의 연결대상 종속회사는 2개사이며, 연결회사의 상호 및 설립일, 주소, 주요사업 등은 다음과 같습니다.
피비파마 한국 사무소
피비파마는 '서울특별시 용산구 한강로동 한강대로 69 에 위치한 용산푸르지오써밋102동 804호'에 한국사무소를 설치하였습니다.

피비파마 대표 바이오 시밀러 2 종
1. 허셉틴 바이오시밀러
- 허셉틴은 대표적인 암 표적치료제로 전이성 유방암뿐만 아니라 초기 위방암 및 전이성 위암 치료에도 사용되며, 연간 글로벌 8조원 이상의 매출을 올리는 블록버스터 의약품입니다. 하지만, 유럽 특허가 2014년 7월 만료되어 2018년 허셉틴 바이오시밀러가 출시되기 시작하였으며, 2019년 6월 허셉틴의 미국 특허가 만료되면서 3조원 규모인 미국 시장의 문도 열렸습니다.
- 허셉틴 바이오시밀러의 경우 당사를 포함한 9개의 경쟁사가 임상 개발 이상의 단계에 있으며, 이 중 피비파마의 의약품을 포함한 7개 의약품이 규제 당국의 판매 승인이 완료 또는 진행 중에 있습니다.
| [허셉틴 바이오시밀러 개발 현황] |
|
1 |
마일란(미국), 바이오콘(인도) |
Ogivri® |
마일란(미국) |
EMA승인(2018) FDA승인(2017) |
유럽 2019.08 |
|
2 |
삼성 바이오에피스(한국) |
Ontruzant® |
대웅제약, 머크(미국) |
EMA승인(2017) FDA승인(2019) |
유럽 2018.03 미국 2020.04 |
|
3 |
셀트리온(한국), 테바(미국) |
Herzuma® |
테바(이스라엘), 먼디파마(EU) |
EMA승인(2018) FDA승인(2018) |
유럽 2018.05 미국 2020.03 |
|
4 |
엘러간(미국), 암젠(미국) |
Kanjinti® |
암젠(미국) |
EMA승인(2018) FDA승인(2019) |
유럽 2018.06 미국 2019.07 |
|
5 |
화이자(미국) |
Trazimera® |
호스피라(미국) |
EMA승인(2018) FDA승인(2019) |
유럽 2019.04 |
| 6 | 상하이 헨리우스(중국), 어코드 (영국) |
Zercepac® | - | EMA승인(2020) | 미정 |
|
7 |
Prestige Biophama(싱가포르) |
Tuzune® |
먼디파마(서유럽), |
EMA신청(2019) |
미정 |
| 8 | Tanvex BioPharma Inc (대만) | TX-05 | - |
임상3상 |
미정 |
| 9 | Gedeon Richter Ltd (헝가리) |
미정 |
- |
임상3상 |
미정 |
2. 아바스틴 바이오시밀러
- 아바스틴은 2004년 판매허가 이후 최근까지 글로벌 매출 10위권에 드는 블록버스터 의약품으로 전이성 대장암, 비소세포폐암 등의 적응증을 보유하고 있습니다. 아바스틴의 미국 특허는 2019년 7월 만료되었으며, 유럽의 경우 2022년 1월 만료가 예정되어 있습니다.
- 피비파마의 HD204(아바스틴 바이오시밀러)는 아바스틴의 유럽 특허가 만료되는 시점인 2022년 출시를 목표로 하고 있으며, 선두주자로 유럽 시장을 선점하여 글로벌 플레이어로 올라설 예정입니다.
| [아바스틴 바이오시밀러 개발 현황] |
|
1 |
엘러간(미국) |
Mvasi® |
암젠(미국) |
EMA승인(2018) FDA승인(2017) |
유럽 미정 |
|
2 |
화이자(미국) |
Zirabev® |
- |
EMA승인(2019) FDA승인(2019) |
유럽 미정 |
| 3 |
삼성바이오에피스(한국) |
Aybintio® |
머크(미국) |
EMA 승인(2020) FDA 신청(2019) |
미정 |
| 4 | Centus Biotherapeutics | Equidacent® | - | EMA 승인(2020) | 미정 |
| 5 |
바이오콘(인도) |
Krabeva® |
마일란(미국) |
FDA 신청 (2020) |
미정 |
| 6 |
Prestige Biophama(싱가포르) |
Vasforda™ |
- |
임상3상 |
미정 |
| 7 | Innovent Biologics (중국) | IBI305 | - | 임상3상 | 미정 |
| 8 |
셀트리온(한국) |
CT-P16 |
- |
임상3상 |
미정 |
| 9 |
Outlook Therapeutics (미국) |
LYTENAVA™ |
비로프로(미국) |
임상3상 |
미정 |
| 10 | Bio-Thera Solutions Ltd(중국) | BAT1706 | - | 임상3상 | 미정 |
|
11 |
닥터 레디 연구소(인도) |
VersavoTM |
- |
임상1상 |
미정 |
|
12 |
아포바이오로직스(캐나다) |
ABX-BEV |
- |
임상1상 |
미정 |
| 13 | Tanvex BioPharma Inc (대만) | TX16 | - | 임상1상 | 미정 |
| 14 | Zhejiang Teruisi Pharmaceutical (중국) |
TRS003 | - | 임상1상 | 미정 |
==============================
포스팅이 도움이 되셨다면
로그인이 필요없는
공감♡ 부탁드립니다.
==============================



